Содержание статьи:
- Причины развития
- Патогенез
- Классификация
- Клиническая картина
- Осложнения
- Диагностика
- Методы лечения
- Прогноз и профилактика
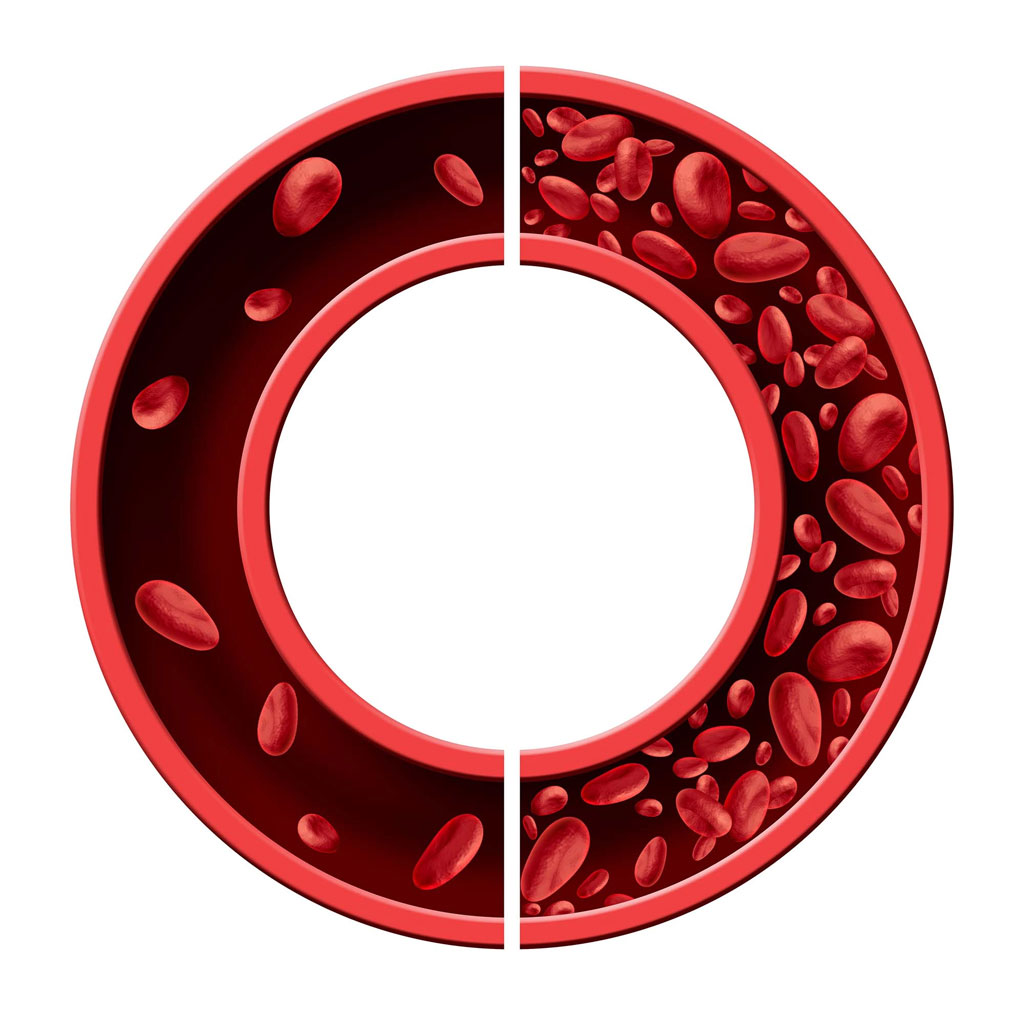
Что такое сидеробластная анемия?
Сидеробластная анемия характеризуется избыточным отложением железа в тканях, при этом его количества не хватает
для синтеза гемоглобина Источник:
Анемии. Сараева
Н.О. Учебное пособие для студентов. Иркутский государственный медицинский университет Федерального
агентства по здравоохранению и социальному развитию. 2009. с.92-97. Болезнь бывает
врожденной и приобретенной. Клиническая картина складывается из анемического синдрома и признаков накопления
железа в органах. Лечение заключается во введении хелатных препаратов для связывания избытков железа,
переливании крови.
Причины развития
Причина врожденной формы сидеробластной анемии — мутации в генах, отвечающих за синтез гемоглобина. Железо, которое должно участвовать в образовании гемоглобина, уходит в ткани и откладывается там.
Причины приобретенной формы анемии:
- миелодиспластический синдром с нарушением кроветворной функции костного мозга;
- онкологические заболевания;
- последствия лучевой терапии, химиотерапии;
- прием гематотоксичных препаратов, прежде всего средств для лечения туберкулеза;
- хроническое отравление свинцом;
- длительное злоупотребление алкоголем;
- аутоиммунные заболевания соединительной ткани.
Повышают риск возникновения сидеробластной анемии курение, работа с химическими веществами, другие анемии, нехватка в рационе витаминов группы В.
Патогенез
В основе формирования сидеробластной анемии лежит нарушение синтеза гемоглобина. Двухвалентное железо и белок протопорфирин образуют гем. Белок глобин связывается с гемом, так образуется гемоглобин. Разные причины анемии ведут к сбоям на разных этапах синтеза гемоглобина:
- нарушение образования протопорфирина;
- нарушение транспортировки гема и глобина.
Даже при достаточном количестве железа в крови формируется гипохромная анемия. Неиспользованное железо оседает в тканях с формированием гемосидероза. Источник:
Клинический случай X-сцепленной сидеробластной анемии с новой миссенс-мутацией cd518 ttg-ttt (leu518phe) в гене alas2. Петренко А.А., Демидова Е.Ю., Сурин В.Л., Стуклов Н.И., Пивник А.В. Гематология и трансфузиология. 2020. №S1. с.198
Классификация
По происхождению сидероахрестическая анемия бывает врожденной и приобретенной. Выделяют несколько видов врожденной анемии в зависимости от типа генетической мутации:
- Х-сцепленные, передаются детям от матерей, нарушена работа гена, ответственного за перенос железа к месту синтеза гемоглобина;
- аутосомно-рецессивная, передается детям лишь в том случае, если оба родителя имеют дефектные гены, ответственные за перенос белка для синтеза гемоглобина;
- митохондриальная цитопатия, при которой происходит мутация в митохондриальной ДНК;
- спорадическая, мутация впервые возникает в семье, где все ее члены здоровы.
Приобретенную анемию тоже классифицируют по причинам возникновения:
- первичная на фоне миелодиспластического синдрома;
- вторичная на фоне онкопатологии, аутоиммунных заболеваний, алкоголизма, отравлений.

Клиническая картина
Симптомы сидеробластной анемии разделяют на два синдрома — гипоксия и гемосидероз. Синдром гипоксии развивается из-за нехватки гемоглобина, который переносит кислород к тканям, характеризуется следующими симптомами:
- утомляемость при обычной нагрузке;
- головокружение;
- приступы одышки;
- эпизоды потери сознания;
- дискомфорт в области сердца;
- сухость, шелушение, бледность кожи;
- выпадение волос, ломкость ногтей;
- нарушение внимания, ухудшение памяти.
Гемосидероз — скопление железа в различных органах, ведущее к нарушению их функции. Накопление железа в печени ведет к воспалению гепатоцитов, орган увеличивается в размере. Начальная стадия гемосидероза печени не имеет ярко выраженных клинических проявлений. Постепенно гепатоциты погибают и формируется цирроз печени. Для этой стадии характерны желтуха, потемнение мочи, боли в правом подреберье, кровоточивость из носа и десен.
Накопление железа в легких приводит к уплотнению легочной ткани, формированию ателектазов. Источник:
Морфология анемий и гемобластозов. Макаров И.Ю., Меньщикова Н.В., Дубяга Е.В., Левченко Н.Р. 2018. Клинически это состояние проявляется чувством нехватки воздуха, одышкой. При поражении более 50% легких формируется дыхательная недостаточность.
Накопление железа в миокарде ведет к увеличению сердца, нарушению ритма. Пациенты ощущают дискомфорт в области сердца, перебои в его работе, чувство тревоги и страха. По мере прогрессирования заболевания формируется сердечная недостаточность. Это состояние проявляется отеками на ногах, одышкой, повышенной утомляемостью, приступами головокружения и потери сознания.
Скопление железа в почках ведет к нарушению их фильтрационной функции. Почки сначала работают в усиленном режиме, что приводит к их гипертрофии. Постепенно часть почечной ткани погибает, формируется почечная недостаточность. Развивается уремическая интоксикация организма. Проявляется это состояние головными болями, повышением давления, отеками на лице. Пациенты отмечают сухость кожи, ломкость ногтей, кожный зуд.
Гемосидероз половых желез у женщин и мужчин становится причиной вторичного бесплодия.
Осложнения
Отсутствие лечения и продолжающееся отложение железа в тканях ведут к необратимому поражению органов, развитию полиорганной недостаточности. Без пожизненного заместительного лечения пациенты с тяжелой сидеробластной анемией погибают. Первичная форма анемии на фоне миелодиспластического синдрома у 5% пациентов приводит к развитию острого лейкоза.
Диагностика
Врач предполагает наличие анемии по характерным для гипоксического синдрома признакам. Дальнейший диагностический поиск направлен на определение характера анемии, выявление причин болезни.
Характерные для сидеробластной анемии изменения в анализах:
- общий анализ крови показывает снижение уровня эритроцитов и цветового показателя, характерны микроцитоз и анизоцитоз. Источник:
Справочник врача общей практики. Палеева Н.Р. Москва: ЭКСПО-Пресс. 2013. с.992; - биохимический анализ показывает высокий уровень ферритина, сывороточного железа, трансферрина на фоне снижения железосвязывающей способности сыворотки;
- генные мутации;
- исследование мочи показывает высокий уровень железа и порфирина;
- исследование костного мозга показывает гиперфункцию эритроцитарного ростка кроветворения.
Ультразвуковое исследование, компьютерная и магнитно-резонансная томография внутренних органов показывают увеличение размеров и плотности вследствие накопления железа.
По результатам обследования пациентам показана консультация гематолога, иммунолога, онколога, генетика.
Методы лечения

Специальная диета при сидеробластной анемии не показана. Рекомендовано включать в рацион продукты, богатые витаминами группы В, аскорбиновой кислотой.
Этиотропное лечение при врожденных формах сидеробластической анемии невозможно. При вторичных приобретенных формах этиотропное лечение заключается в устранении провоцирующего фактора:
- прекращение приема токсичных лекарств;
- выведение из организма отравляющих веществ;
- прекращение употребления алкоголя;
- лечение онкопатологии, аутоиммунных заболеваний.
Патогенетическая и симптоматическая терапия направлены на утилизацию избытков железа в организме, восстановление функции внутренних органов:
- хелатирование — дефероксамин используют для связывания и выведения железа;
- витамин В6 эффективен при пиридоксинзависимых формах анемии;
- гормонотерапия андрогенами, эритропоэтином;
- прием фолиевой кислоты, антиоксидантов, гепатопротекторов.
При снижении гемоглобина менее 70 г/л показано переливание крови, эритроцитарной массы. Хирургическое лечение показано при увеличении селезенки с угрозой ее разрыва, проводят спленэктомию Источник:
Сидеробластные анемии: анемии, вызванные недостаточным эритропоэзом. Дениз М.А. Руководство Merck по диагностике и терапии. 2022. Пациентам с удаленной селезенкой показана пожизненная иммунокорректирующая терапия.
Прогноз и профилактика

Прогноз при первичной и вторичной приобретенной анемии в большинстве случаев благоприятный, пациенты либо излечиваются полностью, либо отмечают значительное улучшение самочувствия. Риск развития осложнений при таких формах болезни минимальный.
Менее благоприятен прогноз при врожденных формах анемии. Нередко уже в детском возрасте пациентам требуются регулярные переливания крови, удаление селезенки. Даже на фоне лечения продолжается накопление железа в тканях, что ведет к развитию полиорганной недостаточности.
Профилактика врожденной сидеробластной анемии заключается в генетическом консультировании пар при планировании беременности. Профилактика приобретенной анемии — здоровый образ жизни, своевременное выявление и лечение онкопатологии и аутоиммунных заболеваний, исключение вредных факторов на производстве.

Источники:
- Анемии. Сараева Н.О. Учебное пособие для студентов. Иркутский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию. 2009. с.92-97
- Клинический случай X-сцепленной сидеробластной анемии с новой миссенс-мутацией cd518 ttg-ttt (leu518phe) в гене alas2. Петренко А.А., Демидова Е.Ю., Сурин В.Л., Стуклов Н.И., Пивник А.В. Гематология и трансфузиология. 2020. №S1. с.198
- Морфология анемий и гемобластозов. Макаров И.Ю., Меньщикова Н.В., Дубяга Е.В., Левченко Н.Р. 2018.
- Сидеробластные анемии: анемии, вызванные недостаточным эритропоэзом. Дениз М.А. Руководство Merck по диагностике и терапии. 2022.
- Справочник врача общей практики. Палеева Н.Р. Москва: ЭКСПО-Пресс. 2013. с.992














 15188
15188